1/ An elegant study from the Sakaguchi and Hori labs explores the role of Foxp3 in Tregs. Despite extensive work, many aspects of Treg biology remain unresolved. this work uncovers another piece of the puzzle.
⬇️
1/ An elegant study from the Sakaguchi and Hori labs explores the role of Foxp3 in Tregs. Despite extensive work, many aspects of Treg biology remain unresolved. this work uncovers another piece of the puzzle.
⬇️
This level of scientific ignorance is unacceptable. You cannot draw conclusions about antigen-specific Treg inhibition from in vitro assays when they do not align with in vivo suppression readouts.
Why do studies claiming #Treg induction by novel designer drugs test them only when given before or with antigen, rather than in established disease that more closely reflects human cases?
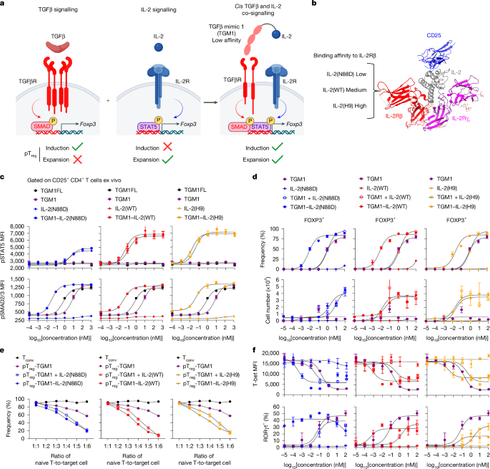
A fusion protein designed to comprise IL-2 and a helminth-derived TGFβ mimic activates IL-2 and TGFβ signalling pathways in IL-2 receptor-expressing T cells and induces stable antigen-specific regulatory T cells in peripheral lymphoid organs.
The exclusive role of RORγt⁺ APCs in inducing or expanding Tregs in the periphery has been challenged. Back to square one.
https://www.biorxiv.org/content/10.64898/2026.02.26.707908v1
The gastrointestinal tract is a unique immunological environment where the host must balance tolerance to commensal microbes with defense against pathogens. A critical mechanism for maintaining this balance is the peripheral conversion of naive T cells into regulatory T cells (pTregs), a process that depends on the TGF-β cytokine, which is produced in a latent form and must be activated. While the activation of latent TGF-β relies on the membrane-bound αvβ8 integrin, the precise cellular subset(s) responsible for this essential process have yet to be clearly defined. Conventional dendritic cells (cDCs), which migrate from the intestinal lamina propria to the gut-draining mesenteric lymph nodes (MLN), have long been considered the primary antigen-presenting cells (APCs) responsible for αvβ8-mediated TGF-β activation and pTreg induction. However, recent studies have challenged this paradigm by highlighting a new family of rare RORγt-expressing APCs, able to induce pTreg via αv integrins, raising questions about the in vivo role of cDCs in the maintenance of mucosal immune homeostasis. Using a β8 integrin gene reporter mouse model (Itgb8-IRES-tdTomato) combined with single-cell profiling, we comprehensively mapped Itgb8-expressing APCs in the MLN. We show that cDCs, in particular migratory type 1 (cDC1) and type 2 (cDC2), constitute the predominant Itgb8(TdTomato)+ cells, both in neonatal and adult mice. Through cDC subset-specific β8 knockout models, we demonstrate that both cDC1 and cDC2 are required for optimal pTreg generation. Loss of β8 integrin in either subset led to a partial reduction in pTreg, while combined deletion resulted in profound pTreg loss and spontaneous colitis. Importantly, these effects were independent of RORγt⁺ APC populations, including ILC3s and Thetis cells. These findings resolve longstanding questions about the identity of key APCs driving pTreg induction in the MLNs. They demonstrate that cDC1 and cDC2 are non-redundant, essential mediators of pTreg induction and intestinal immune tolerance. Although different populations of RORγt⁺ APCs may contribute in specific contexts, such as early development, infection, or in the prevention of allergic disease, cDCs remain one of the primary guardians of intestinal immune homeostasis in response to microbiota. ### Competing Interest Statement The authors have declared no competing interest. Agence Nationale de la Recherche, https://ror.org/00rbzpz17, ANR-20-CE15-0015 Swedish Medical Research Council, 2022-00591 Novo Nordisk Foundation, NNF22OC0071681 Ministere de l'Education Nationale, https://ror.org/04xp49e10, PhD fellowship Agence Nationale de la Recherche, Programme dInvestissements dAvenir, ANR-11-INBS-0013
This study of natural food-specific #Treg development, two years in the making, reveals surprising results that challenge using artificial antigens like OVA. “BioRxiv v2, posted recently, likely signals journal acceptance.
Food antigens elicit immune tolerance through the action of intestinal regulatory T (Treg) cells. Unlike food allergens, the proteins that mediate tolerance are mostly undescribed. Here, we found that epitopes derived from seed storage proteins are targets of murine intestinal Treg cells, with the most frequent response targeting the C-terminus of the maize protein alpha-zein. An MHC tetramer loaded with this antigen revealed that zein-specific T cells are predominantly intestinal Treg cells, develop concurrently with weaning, and constitute up to 2% of the peripheral Treg cell pool. Zein-responsive Treg cells repressed naïve T cell proliferation ex vivo and prior dietary exposure resulted in a constrained response upon multiple inflammatory challenges in vivo, supporting a specific role for gut-resident Treg cells in suppressing systemic immune responses. Together, our work reveals the development, immune suppressive characteristics, and function of naturally occurring Treg cells that recognize dietary seed-storage proteins, a previously undescribed class of antigens in oral tolerance. One-sentence summary Immunodominant epitopes from seed storage proteins are a target of intestinal regulatory T cells that modulate immune challenge to food. ### Competing Interest Statement D.R.L. consults and has equity interest in Vedanta, Immunai, Imidomics, Sonoma Biotherapeutics and Pfizer Pharmaceuticals. M.A.F. is a co-founder of Kelonia and Revolution Medicines, a member of the scientific advisory boards of the Chan Zuckerberg Initiative, Stand Up to Cancer, NGM Biopharmaceuticals, and TCG Labs/Soleil Labs, and an innovation partner at The Column Group. The remaining authors have no conflict of interest. Life Sciences Research Foundation, https://ror.org/0195dxj21 National Science Foundation NIH, F32AI181496 NIH, K08CA283272 Rosenfield and Glassman Foundation ONO Pharma Foundation NIH, R01AI158687 NIH, K99AI173524 NIH, S10RR027431-01 and 1S10OD023831-01
Mary Brunkow’s #FOXP3 discovery earned her a Nobel, though she left the field soon afterward. Douglas Prasher cloned #GFP in 1992, left the field too, and was notably left out of the #Nobel for its discovery.
https://www.science.org/content/article/what-s-it-tell-someone-she-won-nobel-prize
【關鍵專訪】2025諾貝爾醫學獎:「調節性T細胞」像憲兵?相關研究為何曾被認為是「假的」?
julia 2025-10-07 14:13:00 CST2025諾貝爾醫學獎昨(6)日揭曉,由美國學者布朗柯、藍斯德爾以及日本免疫學家坂口志文共享殊榮。究竟研究的內容是什麼?為何學者以「軍隊中的憲兵」來進行比喻?《關鍵評論網》邀請學者就這次獲獎的研究內容進行白話解說。13. In summary: tolerance to self is a fixed, static system established at birth. It does not change dynamically during an individual’s life.
#immunology
#tolerance
#selfnonself
#science
#theory
#Foxp3
#Tregs